FDA одобрила использование еще одной вакцины от COVID-19 в США
17 декабря группа экспертов консультативного совета Управления по санитарному контролю за качеством пищевых продуктов и медикаментов (FDA) рекомендовала разрешить вакцину от COVID-19 компании Moderna для использования во время пандемии. Это решение открыло путь для шести миллионов доз, которые будут отправлены уже 19 и 20 декабря, пишет NDTV.
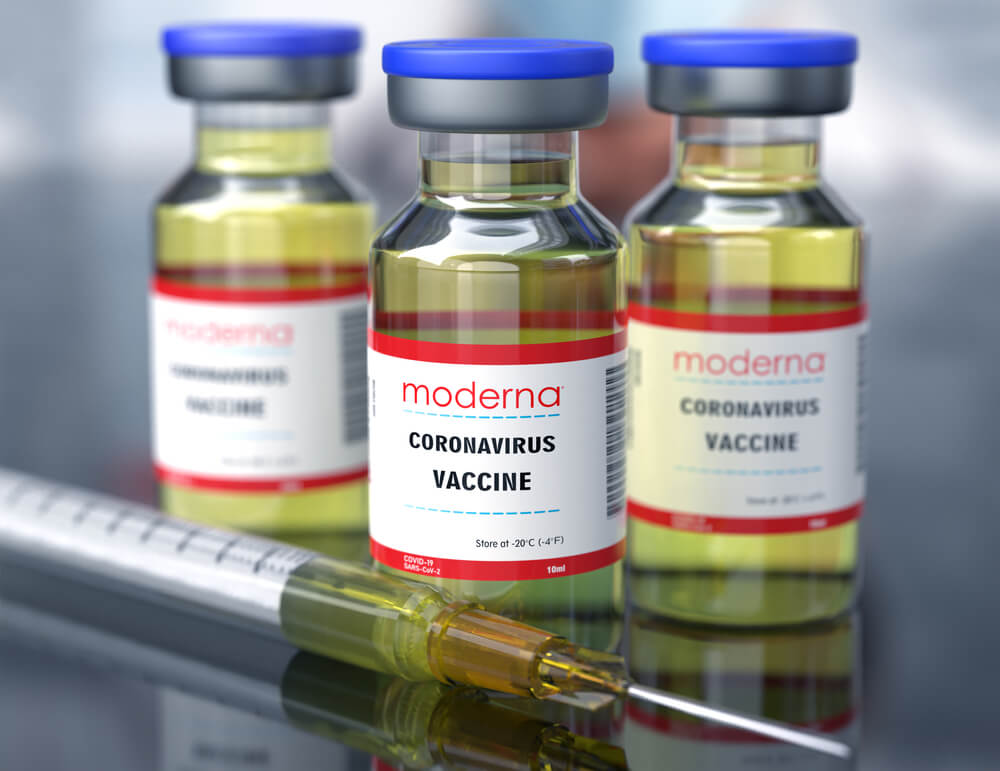
Фото: Shutterstock
Теперь ожидается, что в ближайшее время FDA выдаст официальное разрешение на использование ее в чрезвычайных ситуациях (EUA), что сделает вакцину Moderna вторым таким препаратом, одобренным в западной стране.
Двадцать голосующих членов группы выступили «за» и один воздержался. «Против» не проголосовал никто.
Их попросили ответить на вопрос: «Основываясь на совокупности имеющихся научных данных, перевешивают ли преимущества вакцины Moderna от COVID-19 ее риски при использовании у лиц в возрасте 18 лет и старше?»
Встреча консультативного совета состоялась в период, когда число смертей от коронавирусной инфекции стремительно приближается к 310 000 в наиболее пострадавшей стране в мире, которая 14 декабря начала вакцинацию медицинских работников и пациентов длительного ухода вакциной Pfizer/BioNTech.
По теме: В США началась вакцинация от COVID-19: как подготовиться и чего ожидать
Обе одобренные вакцины основаны на передовой технологии мРНК (мессенджер рибонуклеиновой кислоты), и обе требуют схемы введения, включающей две дозы.
Хотя уровень защиты от COVID-19 для обеих вакцин составляет 94-95% — намного больше, чем думали эксперты, — в настоящее время во всем мире есть несколько людей, у которых после вакцинации Pfizer развились серьезные аллергические реакции.
США, где зарегистрированы более 17 миллионов случаев заражения вирусом, вероятно, станут первой страной, одобрившей вакцину Moderna. Небольшая биотехнологическая фирма из Массачусетса объединилась с учеными из Национального института здоровья США в работе над продуктом и получила более 2,5 миллиарда долларов от правительства США на свои усилия.
Защита от инфекции
Клиническое испытание с участием 30 400 человек показало, что эффективность вакцины в предотвращении COVID-19 составляет 94,1% по сравнению с плацебо; у молодых людей она несколько выше, чем у пожилых.
По словам Жаклин Миллер, вице-президента Moderna по развитию инфекционных заболеваний, у экспертов есть серьезные основания полагать, что вакцина защитит большинство людей от инфекции, что важно с точки зрения общественного здравоохранения, поскольку она предотвратит дальнейшую передачу.
Обзор всех доступных данных FDA показал, что «не было выявлено особых проблем с безопасностью препарата».
Но 17 декабря официальный представитель FDA Доран Финк сказал, что в случае выдачи EUA агентство выпустит специальную этикетку с предупреждением о потенциальных аллергических реакциях (к таким мерам хотят прибегнуть после того, как у двух медицинских работников на Аляске возникла подобная реакция на вакцину Pfizer, и одного из них госпитализировали. У двух медицинских работников в Великобритании также были аллергические реакции.
Вам может быть интересно: главные новости Нью-Йорка, истории наших иммигрантов и полезные советы о жизни в Большом Яблоке – читайте все это на ForumDaily New York
Дилемма с плацебо
Moderna подверглась критике со стороны Стэнфордского эксперта Стивена Гудмана из-за ее планов предложить вакцину участникам испытания, получившим плацебо, даже до того, как она станет общедоступной для их демографической группы.
По его словам, это лишит испытание контрольной группы и снизит качество данных, которые можно было бы извлечь из него, а также создаст плохой прецедент для будущих испытаний.
Но Тал Закс, главный врач Moderna, поддержал это предложение.
«Ни один из участников нашего испытания не станет «перепрыгивать» других, потому что у нас есть запасы материалов для клинических испытаний, срок годности которых истекает, их и расходуем», — сказал он, а затем сообщил, что участники находятся в группе высокого риска, один человек из группы плацебо даже умер от тяжелой формы COVID-19.
Побочные эффекты
Наиболее частыми побочными эффектами, связанными с препаратом мРНК-1273, были: боль в месте инъекции, слабость, головная боль, боль в мышцах и в суставах , озноб.
Некоторые из этих симптомов были классифицированы как «серьезные».
Аллергические реакции возникли у 1,5% вакцинированных по сравнению с 1,1% в контрольной группе, но ни одна из них не была классифицирована как тяжелая.
По теме: Pfizer опубликовала отчет о побочных эффектах вакцины от COVID-19
На сегодняшний день известно о трех случаях паралича Белла (паралича лицевого нерва, чаще всего временного) в группе вакцинированных и одном — в группе плацебо.
В FDA заявили, что нет достаточной информации для определения того, была ли причиной паралича вакцинация, но наблюдение продолжается.
Читайте также на ForumDaily:
Джо Байден вакцинируется от COVID-19 на камеру: почему Трамп не делает прививку
Чай, шоколад, вино: еда может снизить риск заражения коронавирусом
Наживаются на страхе: в США мошенники распространяют дезинформацию о вакцине от COVID-19
Трамп предложил отложить вакцинацию сотрудников Белого дома от COVID-19
Подписывайтесь на ForumDaily в Google NewsХотите больше важных и интересных новостей о жизни в США и иммиграции в Америку? — Поддержите нас донатом! А еще подписывайтесь на нашу страницу в Facebook. Выбирайте опцию «Приоритет в показе» — и читайте нас первыми. Кроме того, не забудьте оформить подписку на наш канал в Telegram и в Instagram— там много интересного. И присоединяйтесь к тысячам читателей ForumDaily New York — там вас ждет масса интересной и позитивной информации о жизни в мегаполисе.